
პლუტონიუმი
ქიმიური ელემენტი / From Wikipedia, the free encyclopedia
პლუტონიუმი[1][2] (ლათ. Plutonium; ქიმიური სიმბოლო — 










| პლუტონიუმი |
| 94Pu |
| [244] |
| 5f6 7s2 |
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ზოგადი თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| მარტივი ნივთიერების ვიზუალური აღწერა | ბზინვარე თეთრი ლითონი | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მასური რიცხვი | 244 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| პლუტონიუმი პერიოდულ სისტემაში | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომური ნომერი (Z) | 94 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| პერიოდი | 7 პერიოდი | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ბლოკი |
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტრონული კონფიგურაცია | [Rn] 5f6 7s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტრონი გარსზე | 2, 8, 18, 32, 24, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
ელემენტის ატომის სქემა | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ფიზიკური თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| აგრეგეგატული მდგომ. ნსპ-ში | მყარი სხეული | |||||||||||||||||||||||||||||||||||||||||||||||||||
| დნობის ტემპერატურა |
639.4 °C (912.5 K, 1182.9 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| დუღილის ტემპერატურა |
3228 °C (3505 K, 5842 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| სიმკვრივე (ო.ტ.) | 19.85 (239Pu) გ/სმ3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| სიმკვრივე (ლ.წ.) | 16.63 გ/სმ3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| დნობის კუთ. სითბო | 2.82 კჯ/მოლი | |||||||||||||||||||||||||||||||||||||||||||||||||||
| აორთქ. კუთ. სითბო | 333.5 კჯ/მოლი | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მოლური თბოტევადობა | 35.5 ჯ/(მოლი·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||
ნაჯერი ორთქლის წნევა
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომის თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ჟანგვის ხარისხი | +2, +3, +4, +5, +6, +7, +8 (an amphoteric oxide) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტროდული პოტენციალი |
Pu←Pu4+ −1.25 ვ Pu←Pu3+ −2.0 ვ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ელექტროუარყოფითობა | პოლინგის სკალა: 1.28 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| იონიზაციის ენერგია |
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| ატომის რადიუსი | ემპირიული: 159 პმ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| კოვალენტური რადიუსი (rcov) | 187±1 პმ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მოლური მოცულობა | 12.12 სმ3/მოლი | |||||||||||||||||||||||||||||||||||||||||||||||||||
|
პლუტონიუმის სპექტრალური ზოლები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| სხვა თვისებები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ბუნებაში გვხვდება | დაშლის შედეგად | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მესრის სტრუქტურა |
მონოსოლური 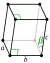 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მესრის პერიოდი | 10.963 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ბგერის სიჩქარე | 2260 მ/წმ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| თერმული გაფართოება | 46.7 µმ/(მ·K) (25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ხვედრითი თბოტევადობა | 32.77 ჯ/(K·მოლ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| თბოგამტარობა | 6.74 ვტ/(მ·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| მაგნეტიზმი | პარამაგნეტიკი | |||||||||||||||||||||||||||||||||||||||||||||||||||
| იუნგას მოდული | 96 გპა | |||||||||||||||||||||||||||||||||||||||||||||||||||
| წანაცვლების მოდული | 43 გპა | |||||||||||||||||||||||||||||||||||||||||||||||||||
| პუასონის კოეფიციენტი | 0.21 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS ნომერი | 7440-07-5 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| ისტორია | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| სახელწოდება მომდინარეობს | პლანეტა „პლუტონის“ სახელის მიხედვით | |||||||||||||||||||||||||||||||||||||||||||||||||||
| აღმომჩენია | გ. სიბორგი, ე. მაკილანი, ჯ. კენედი და ა. ვალი (1940-1941) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| პლუტონიუმის მთავარი იზოტოპები | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| • | ||||||||||||||||||||||||||||||||||||||||||||||||||||
ელემენტს ახასიათებს სხვა ელემენტებისაგან განსხვავებული სტრუქტურული და ფიზიკო-ქიმიური თვისებები. პლუტონიუმს გააჩნია შვიდი ალოტროპიული მოდიფიკაცია გარკვეულ ტემპერატურასა და წნევების დიაპაზონში: α, β, γ, δ, δ', ε და ζ. შეუძლია მიიღოს ჟანგვის ხარისხები +2-დან +7-მდე, ძირითადად მიიჩნევა +4, +5, +6. სიმკვრივე ვარირებს 19,8-დან (α-Pu) 15,9 გრ/სმ³-მდე (δ-Pu).
პლუტონიუმს სტაბილური იზოტოპები არ გააჩნია. ბუნებაში არის კვალის რაოდენობით. ყველა ტრანსურანულ ელემენტებს შორის ყველაზე ხანგრძლივად მცხოვრები იზოტოპებია 244Pu, 239Pu და 238Pu. ბუნებაში უპირატესად არის პლუტონიუმ (IV) ოქსიდის (PuO2) დიოქსიდის სახით, რომელიც წყალში უფრო ნაკლებად ხსნადია ვიდრე ქვიშა (კვარცი). ელემენტის ბუნებაში არსებობა იმდენად მცირეა, რომ მისი მოპოვება არამიზანშეწონილია, შეფარდება 
პლუტონიუმის მისაღებად გამოიყენება როგორც გამდიდრებული ურანი ისე ბუნებრივი ურანი. მსოფლიოში სხვადასხვა ფორმით არსებული პლუტონიუმის მთლიანი რაოდენობა, ფასდება 2003 წ. - 1239 ტ. 2010 წელს ეს ციფრი გაიზარდა ~2000 ტ-მდე[3].
ფართოდ გამოიყენება ბირთვული იარაღის წარმოებაში (ე. წ. „იარაღის პლუტონიუმი“), ბირთვულ საწვავად სამოქალაქო და კვლევითი დანიშნულების ატომურ რეაქტორებში და როგორც ენერგიის წყარო კოსმოსური აპარატებისათვის[4]. იყო შეტყობინება მსოფლიოში ბოლო იარაღის პლუტონიუმის მისაღები ბირთვული რეაქტორის დახურვის შესახებ АДЭ-2, რომელიც ამეშავებდა 46 წელს და გაჩერებულ იქნა 2010 წ. აპრილში რუსეთში[5][6][7], თუმცა ერთი თვის შემდეგ იაპონიაში გაშვებულ იქნა რეაქტორი „მონძიუ“[8][9]. კონფლიქტისა და შუღლის გამო კორეის რესპუბლიკასა და კორეის სახალხო დემოკრატიულ რესპუბიკას შორის, ბოლომ მიმართა ორ მიწისქვეშა ბირთვულ გამოცდას 2006 წ-ის ოქტომბერში და 2009 წწ მაისში. საკუთარი ბირთვული პროგრამის ფარგლებში რომელიც ეფუძნებოდა პლუტონიუმს[10][11][12].
მეორე ნეპტუნიუმის შემდეგ (შეცდომით იქნა „მიღებული“ 1934 წელს ე. ფერმის ჯგუფის მიერ[13]; პირველი იზოტოპი 239Np სინთეზირებულ და იდენტიფიცირებულ იქნა 1940 წლის მაისში ე. მიკმილანის და ფ. აბელსონის მიერ[14][15][16]) ხელოვნური ელემენტი იყო პლუტონიუმი, მიღებული მიკროგრამული რაოდენობით 1940 წ-ის ბოლოს იზოტოპ 238Pu-ის სახით. პირველი ხელოვნური ქიმიური ელემენტი, რომლის საწარმოო მასშტაბით წარმოება იქნა დაწყებული (სსრკ 1946 წ ჩელიაბინსკ-40 შექმნილი იქნა რამდენიმე საწარმო იარაღის ურანის და პლუტონიუმის საწარმოებლად[17]). პირველ ბირთვულ ბომბში მსოფლიოში, რომელიც შეიქმნა და გამოიცადა 1945 წელს აშშ-ში, გამოიყენებოდა პლუტონიუმის მუხტი. ასეთივე ტიპის იყო სსრკ-ში გამოცდილი პირველი ბომბა 1949 წელს[18]. შესაბამისად აშშ, ხოლო შემდეგ სსრკ იყვნენ პირველი ქვეყნები რომლებმაც აითვისეს მისი მიღება.
ცხრილში მოყვანილია α-პლუტონიუმის ძირითადი თვისებები. ეს ალოტროპიული მოდიფიკაცია პლუტონიუმისათვის წარმოადგენს ძირითადს ოთახის ტემპერატურაზე და ნორმალური წნევისას.
CAS ნომერი:
- 7440-07-5 არასპეციფიკური შემადგენლობის პლუტონიუმისათვის,
- 13981-16-3 238Pu-თვის,
- 15117-48-3 239Pu-თვის,
- 14119-33-6 240Pu-თვის.