
Trifluorure de chlore
composé chimique / De Wikipedia, l'encyclopédie encyclopedia
Cher Wikiwand IA, Faisons court en répondant simplement à ces questions clés :
Pouvez-vous énumérer les principaux faits et statistiques sur Trifluorure de chlore?
Résumez cet article pour un enfant de 10 ans
Le trifluorure de chlore est un interhalogène de formule ClF3. C'est un gaz incolore, très oxydant et extrêmement réactif, corrosif et toxique, qui se condense en un liquide jaune verdâtre. C'est sous sa forme liquide pressurisée à température ambiante qu'on le trouve le plus souvent sur le marché. On s'en sert surtout dans les phases de nettoyage et pour les gravures chimiques dans l'industrie des semiconducteurs[5],[6], et dans quelques autres processus industriels[7]. Il est notamment utilisé dans le cycle du combustible nucléaire[8], où il permet la conversion des composés fluorés d'uranium non volatils en hexafluorure d'uranium UF6, composé aux propriétés physiques intéressantes du point de vue des procédés d'enrichissement de l'uranium :
| Trifluorure de chlore | |||
   |
|||
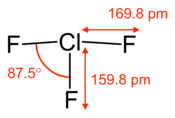
| Structure du trifluorure de chlore. | |||
| Identification | |||
|---|---|---|---|
| No CAS | 7790-91-2 | ||
| No ECHA | 100.029.301 | ||
| No CE | 232-230-4 | ||
| No RTECS | FO2800000 | ||
| PubChem | 24637 | ||
| ChEBI | 30123 | ||
| SMILES | |||
| InChI | |||
| Apparence | Gaz ou liquide jaunâtre | ||
| Propriétés chimiques | |||
| Formule | ClF3 [Isomères]ClF3 | ||
| Masse molaire[1] | 92,448 ± 0,002 g/mol Cl 38,35 %, F 61,65 %, |
||
| Moment dipolaire | 0,6 ± 0,1 D[2] | ||
| Propriétés physiques | |||
| T° fusion | −76,31 °C[3] | ||
| T° ébullition | 11,8 °C[3] | ||
| Masse volumique | 3,57 kg·m-3[3] à 0 °C et 101,3 kPa | ||
| Pression de vapeur saturante | 141,9 kPa[3] à 20 °C | ||
| Point critique | 174,0 °C ; 5,78 MPa ; 0,548 g·cm-3[3] | ||
| Point triple | −76,3 °C[3] | ||
| Thermochimie | |||
| ΔvapH° | 27,53 kJ·mol-1 (1 atm, 11,75 °C)[4] | ||
| Précautions | |||
| SGH[3] | |||
| H270, H280, H314, H330, H370, H372 et H400 H270 : Peut provoquer ou aggraver un incendie ; comburant H280 : Contient un gaz sous pression ; peut exploser sous l'effet de la chaleur H314 : Provoque de graves brûlures de la peau et des lésions oculaires H330 : Mortel par inhalation H370 : Risque avéré d'effets graves pour les organes (ou indiquer tous les organes affectés, s'ils sont connus)(indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H372 : Risque avéré d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H400 : Très toxique pour les organismes aquatiques |
|||
| Transport[3] | |||
Code Kemler : 265 : gaz toxique et comburant (favorise l'incendie) Numéro ONU : 1749 : TRIFLUORURE DE CHLORE Classe : 2.3 Étiquettes :  2.3 : Gaz toxiques (correspond aux groupes désignés par un T majuscule, c'est-à-dire T, TF, TC, TO, TFC et TOC).  5.1 : Matières comburantes  8 : Matières corrosives Emballage : - |
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Son utilisation comme comburant pour la propulsion spatiale est aujourd'hui abandonnée compte tenu des risques réels pour le matériel et pour les équipages ; c'est en revanche la matière première pour la synthèse du pentafluorure de chlore ClF5, un ergol parfois employé, le plus souvent avec l'hydrazine, pour la propulsion de certains missiles[9].



