
Perklorata acido
kemia kombinaĵo / From Wikipedia, the free encyclopedia
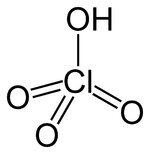
Perklorata acido aŭ HClO4 estas klora oksoacido, substanco oleeca kaj senkolora, solvebla en akvo kaj akrodora. La kloro de la perklorata acido prezentas oksidastato +7. En koncentriĝoj pli altaj ol 72% ĝi facile eksplodas, tiamaniere ke ĝi malfacile estigeblas pura, do, ĝi estas komercita laŭ ĝia akva solvaĵo maksimume kun koncentriĝo 70%. La perklorata acido estas unubaza acido:
| Perklorata acido | |||||
 | |||||
 | |||||
| Alternativa(j) nomo(j) | |||||
| Hidrogena perklorato | |||||
| Kemia formulo | HClO4 | ||||
| PubChem-kodo | 24247 | ||||
| ChemSpider kodo | 22669 | ||||
| CAS-numero-kodo | 7601-90-3 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora senodora likvaĵo | ||||
| Molmaso | 100.46 g mol−1 | ||||
| Smiles | OCl(=O)(=O)=O | ||||
| Denseco | 1.768 g/cm3 (likva) | ||||
| Fandopunkto | −17 °C (1 ℉; 256 K) (azeotropa) | ||||
| Bolpunkto | 203 °C (397 ℉; 476 K) | ||||
| Solvebleco | Akvo:Tute solvebla | ||||
| Acideco (pKa) | -10 | ||||
| Sekurecaj Indikoj | |||||
| Risko | |||||
| Sekureco | |||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj[1][2] | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝo | ||||
| GHS Deklaroj pri damaĝoj | H271, H290, H302, H314, H373 | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P220, P260, P280, P303+361+353, P304, P305+351+338, P310, P340, P371+380+375 | ||||
(25 °C kaj 100 kPa) | |||||
HClO4 • H2O → [H3O]+ + [ClO4]−
Koncentriĝoj pli altaj ol 70% iom post iom okazas formiĝo de "perklorata anhidrido" Cl2O7, kaj sekve oni konstatas eksplododanĝeron per la reakcio:
3 HClO4 → [H3O]+ + [ClO4]− + Cl2O7
Kune kun akvo la perklorata acido formas azeotropan miksaĵon bolanta je 203 °C, en kiu ĉeestas koncentriĝon je 28.4%. Sub ĉi-kondiĉo la acido restas sendifine stabila kaj komerce disponeblas. Ĝiaj solvaĵoj estas higroskopaj, t. e., la solvaĵoj konstante diluiĝos per absorbado de la akvo el la atmosfero, kiam ili ne estas firme enfermita. Ĝi estas forta acido kiam komparata al sulfata acido kaj nitrata acido. Ĝi estas superacido, sed ne tiel forta kiel la acido de Brønsted-Lowry, tiel kiel la fluoroantimona acido aŭ HFSbF5.







