Молекулска орбитала
таласасто понашање електрона у молекулу / From Wikipedia, the free encyclopedia
У хемији, молекулска орбитала (скр. МО) је математичка функција која описује понашање електрона као таласа у молекулу.[1][2][3] Ова функција се може користити за израчунавање физичких и хемијских особина као што је налажење електрона у одређеном делу простора. Молекулске орбитале се најчешће конструишу комбинацијом атомских или хибридних орбитала сваког од атома у датом молекулу.[4][5] Термине атомска орбитала и молекуларна орбитала[lower-alpha 1] увео је Роберт С. Маликен 1932. да означавају једноелектронске орбиталне таласне функције.[7] На елементарном нивоу, они се користе за описивање области простора у којој функција има значајну амплитуду.
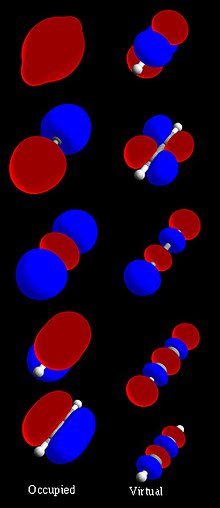
На елементарном нивоу, молекулска орбитала се користи за описивање простора у коме функција има значајну амплитуду. У изолованом атому локација орбиталних електрона одређена је функцијама које се називају атомске орбитале. Када се више атома хемијски комбинује у молекул, локације електрона одређују молекул у целини, тако да се атомске орбитале комбинују и формирају молекуларне орбитале. Електрони из саставних атома заузимају молекуларне орбитале. Математички, молекуларне орбитале су приближно решење Шредингерове једначине за електроне у пољу атомских језгара молекула. Оне се обично граде комбинујући атомске орбитале или хибридне орбитале из сваког атома молекула или друге молекуларне орбитале из група атома. Оне се могу квантитативно израчунати помоћу Хартри-Фокововог или метода самоконзистентних поља ().