
Metan
From Wikipedia, the free encyclopedia
Metan (CH4), poznat i kao blatni gas je najprostiji zasićeni ugljovodonik (alkan). Ukoliko vladaju normalni uslovi on je bezbojan gas.
| Metan | |
|---|---|
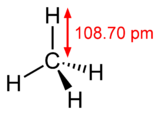 |
 |
 |
 |
| Drugi nazivi | Metil hidrid, biogas |
| Identifikacija | |
| CAS registarski broj | 74-82-8 |
| PubChem[1][2] | 297 |
| ChemSpider[3] | 291 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | CH4[4] |
| Molarna masa | 16.042 g/mol |
| Agregatno stanje | Bezbojni gas |
| Gustina | 0.717 kg/m3 (gas, 0 °C) 415 kg/m3 (tečnost) |
| Tačka topljenja |
-182.5 °C, 91 K, -297 °F |
| Tačka ključanja |
-161.6 °C, 112 K, -259 °F |
| Rastvorljivost u vodi | 35 mg/L (17 °C) |
| Opasnost | |
| Opasnost u toku rada | Visoko zapanjiv (F+) |
| NFPA 704 | |
| R-oznake | R12 |
| S-oznake | S2, S9, S16, S33 |
| Tačka paljenja | -188 °C |
| Eksplozivni limiti | 5 – 15% [5] |
| Srodna jedinjenja | |
| Srodna Alkanii | Etan, propan |
| Сродна једињења | Metanol, Hlorometan, Mravlja kiselina, formaldehid, silan |
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |
| Infobox references | |
U prirodi metan nastaje usled bezkiseoničnog raspada organskih materija (npr. močvarama). Metan je glavni sastojak zemnog gasa. Koristi se kao gas za grejanje i kao sirovina za dobijanje organskih jedinjenja
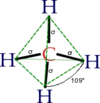
Molekul metana ima oblik tetraedra. Atom ugljenika s ima sp3 hibridizaciju. Ostale orbitale grade hemijsku vezu sa četri atoma vodonika. Sve četri veze su podjednake (uglovi između veza iznose 109°28') i veoma su malo polarizovane, što je zajedno sa nedostatkom slobodnih elektronskih parova velike postojanosti ovog jedinjenja. Metan može da učestvuje samo u reakcijama tipičnim za alkane (npr: sagorjevanje).
Labaratorijski metan se dobija prženjem natrijum acetata sa natrijum hidroksidom:
- CH3COONa + NaOH → CH4 + Na2CO3
Druga metoda je hidroliza aluminijum karbida:
- Al4C3 +12H2O → 3CH4 + 4Al(OH)3
