
암모니아
질소와 수소로 이루어진 화합물 / From Wikipedia, the free encyclopedia
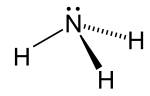
암모니아(영어: ammonia)는 질소와 수소로 이루어진 화합물로 분자식은 NH3이다. 끓는점이 약 -33도이므로 실온에서 기체 상태로 존재한다.[12] 특유의 자극적인 냄새가 나며 무색이다. 대기 중에 소량이 존재하며, 천연수에도 미량 함유되어 있다. 토양 중에도 세균의 질소 유기물의 분해 과정에서 생겨난 암모니아가 존재할 수 있다.[13] 대표적인 반자성체 중 하나이다.
 | |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름 | |||
| 별칭
azane (only intended for use in naming derivatives of ammonia), hydrogen nitride, R-717 (refrigerant), R717 (refrigerant alternative spelling) | |||
| 식별자 | |||
3D 모델 (JSmol) |
|||
| 3DMet | |||
| 3587154 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider |
| ||
| ECHA InfoCard | 100.028.760 | ||
| EC 번호 |
| ||
| 79 | |||
| KEGG |
| ||
| MeSH | Ammonia | ||
PubChem CID |
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1005 | ||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| 성질 | |||
| NH3 | |||
| 몰 질량 | 17.031 g/mol | ||
| 겉보기 | 무색 기체 | ||
| 냄새 | strong pungent odour | ||
| 밀도 | 0.86 kg/m3 (1.013 bar at boiling point) 0.769 kg/m3 (STP)[2] | ||
| 녹는점 | −77.73 °C (−107.91 °F; 195.42 K) (삼중점은 6.060 kPa, 195.4 K) | ||
| 끓는점 | −33.34 °C (−28.01 °F; 239.81 K) | ||
| 임계점 (T, P) | 132.4 °C (405.5 K), 111.3 atm (11,280 kPa) | ||
| 47% w/w (0 °C) 31% w/w (25 °C) 18% w/w (50 °C)[5] | |||
| 용해도 | 클로로포름, 다이에틸 에터, 에탄올, 메탄올에 용해된다 | ||
| 증기 압력 | 857.3 kPa | ||
| 산성도 (pKa) | 32.5 (−33 °C),[6] 10.5 (DMSO) | ||
| 염기도 (pKb) | 4.75 | ||
| 짝산 | 암모늄 이온 | ||
| 짝염기 | Amide | ||
자화율 (χ) |
−18.0·10−6 cm3/mol | ||
굴절률 (nD) |
1.3327 | ||
| 점도 |
| ||
| 구조 | |||
점군 |
C3v | ||
| 삼각뿔형 | |||
| 1.42 D | |||
| 열화학 | |||
표준 몰 엔트로피 (S |
193 J·mol−1·K−1[8] | ||
표준 생성 엔탈피 (ΔfH⦵298) |
−46 kJ·mol−1[8] | ||
| 위험 | |||
| 물질 안전 보건 자료 | ICSC 0414 (anhydrous) | ||
| GHS 그림문자 |    [9] [9] | ||
| 신호어 | 위험 | ||
GHS 유해위험문구 |
H290, H301, H311, H314, H330, H334, H336, H360, H362, H373, H400 | ||
GHS 예방조치문구 |
P202, P221, P233, P261, P263, P271, P273, P280, P305+351+338, P310[9] | ||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 132 | ||
| 651 °C (1,204 °F; 924 K) | |||
| 폭발 한계 | 15–28% | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose) |
0.015 mL/kg (human, oral) | ||
LC50 (median concentration) |
40,300 ppm (rat, 10 min) 28,595 ppm (rat, 20 min) 20,300 ppm (rat, 40 min) 11,590 ppm (rat, 1 hr) 7338 ppm (rat, 1 hr) 4837 ppm (mouse, 1 hr) 9859 ppm (rabbit, 1 hr) 9859 ppm (cat, 1 hr) 2000 ppm (rat, 4 hr) 4230 ppm (mouse, 1 hr)[10] | ||
LCLo (lowest published) |
5000 ppm (mammal, 5 min) 5000 ppm (human, 5 min)[10] | ||
| NIOSH (미국 건강 노출 한계):[11] | |||
PEL (허용) |
50 ppm (25 ppm ACGIH- TLV; 35 ppm STEL) | ||
REL (권장) |
TWA 25 ppm (18 mg/m3) ST 35 ppm (27 mg/m3) | ||
IDLH (직접적 위험) |
300 ppm | ||
| 관련 화합물 | |||
다른 양이온 |
포스핀 아르신 Stibine Bismuthine | ||
관련 nitrogen hydrides |
하이드라진 Hydrazoic acid | ||
관련 화합물 |
암모니아수 | ||
암모니아는 강한 부식성이 있는 맹독성 물질이며, 물에 잘 흡수되는 특성이 있다.[14] 따라서 고농도의 암모니아에 노출될 경우에 점막에 급격히 흡수되어 세포 조직을 치명적으로 파괴하기 때문에 눈, 코, 입, 귀를 막고 신속히 현장을 이탈해야 한다.
20세기 초에 프리츠 하버가 공기 중의 질소를 이용한 암모니아 합성법을 개발하였고[15] 이를 통해 요소 비료를 대량생산 하게 되었다. 이로써 식물의 성장을 위한 단백질 합성에 필수 요소인 질소를 저렴한 가격의 화학 비료를 통해 토양에 공급할 수 있게 되었고, 곡물 생산성이 크게 향상되어 인류는 굶주림의 공포에서 해방되었다.
암모니아는 냉매, 용매, 소독세정제로 이용되고 합성수지 제조 등 화학공업의 다양한 분야에 널리 사용되고 있다.


