
نیتروز اکسید
گاز غیر قابل اشتعال بیرنگ / From Wikipedia, the free encyclopedia
دینیتروژن مونوکسید یا نیتروز اکسید یا گاز خنده (N۲O) یکی از ترکیبات نیتروژن است که اولین بار در سال ۱۷۹۹ در دندانپزشکی استفاده شد. امروزه از آن در پزشکی برای القا و ادامهٔ بیهوشی استفاده میشود. این دارو همچنین با مقادیر مصرف کم بهعنوان ضد درد در اعمال جراحی زنان و زایمان و برای عمل جراحی که در آنها به بیهوشی کامل بیمار نیاز نیست، مصرف میشود. این گاز یک مادهٔ سایکو اکتیو از نوع منفک کننده است که در جوامع غربی به صورت گسترده به منظور ایجاد حس سرخوشی و توهم مورد مصرف قرار میگیرد بهطوری که تخمین زده میشود در سال ۲۰۱۴ توسط نیم میلیون جوان بریتانیایی مصرف شده باشد.[1]
| نیتروز اکسید | |
|---|---|
 | |
 | |
Dinitrogen monoxide | |
دیگر نامها Laughing gas sweet air | |
| شناساگرها | |
| شماره ثبت سیایاس | ۱۰۰۲۴-۹۷-۲ |
| پابکم | ۹۴۸ |
| کماسپایدر | ۹۲۳ |
| UNII | K50XQU1029 |
| شمارهٔ یواِن | 1070 (compressed) 2201 (liquid) |
| KEGG | D00102 |
| ChEBI | CHEBI:17045 |
| ChEMBL | CHEMBL۳۳۵۹۰۰ |
| شمارهٔ آرتیئیسیاس | QX1350000 |
| کد اِیتیسی | N01AX13 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | N2O |
| جرم مولی | 44.013 g/mol |
| شکل ظاهری | colorless gas |
| چگالی | 1.977 g/L (gas) |
| دمای ذوب | −۹۰٫۸۶ °C (182.29 K) |
| دمای جوش | −۸۸٫۴۸ °C (184.67 K) |
| انحلالپذیری در آب | 0.15 g/100 ml (15 °C) |
| انحلالپذیری | soluble in الکل، اتر، سولفوریک اسید |
| log P | 0.35 |
| فشار بخار | 5150 kPa (20 °C) |
| ضریب شکست (nD) | 1.330 |
| ساختار | |
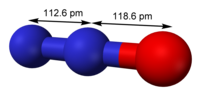
| شکل مولکولی | linear C∞v |
| گشتاور دوقطبی | 0.166 D |
| ترموشیمی | |
آنتروپی مولار استاندارد S |
219.96 J K-1 mol-1 |
آنتالپی استاندارد تشکیل ΔfH |
+82.05 kJ/mol |
| داروشناسی | |
| Routes of administration |
دم (تنفس) |
| دگرگشت | 0.004% |
| Elimination half-life |
5 minutes |
| دفع | دستگاه تنفسی |
| ردهبندی داروهای بارداری | |
| خطرات | |
| MSDS | Ilo.org, ICSC 0067 |
| شاخص ئییو | Oxidant [O] |
| لوزی آتش | |
| نقطه اشتعال | |
| ترکیبات مرتبط | |
| مرتبط با نیتروژن اکسید | نیتریک اکسید دینیتروژن تریاکسید نیتروژن دیاکسید دینیتروژن تترااکسید دینیتروژن پنتاکسید |
| ترکیبات مرتبط | آمونیوم نیترات آزید |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
نیتروز اکسید (N۲O) گازی بیرنگ، بیبو و غیرقابل اشتعال است. N۲O سمّی نیست اما خندهآور است. این گاز در ردهٔ اصلی گازهای گلخانهای قرار داشته و آلوده کنندهٔ هوا میباشد. مطالعات اخیر نشان میدهد که این گاز میتواند باعث آسیب به سلولهای عصبی شود[2] و پزشکان نسبت به مصرف آن در بین عموم هشدار دادهاند.[3]
همچنین در موتورهای موشکی نیز کاربرد دارد اکسید نیتروژن ممکن است به عنوان یک اکسید کننده در موتور موشک استفاده شود. مزایایی نسبت به سایر اکسید کنندهها دارد زیرا سمی بسیار کمتری دارد و به دلیل پایداری در دمای اتاق ذخیرهسازی آسانتر و حمل در پرواز نسبتاً ایمن است. به عنوان یک مزیت ثانویه، ممکن است به راحتی تجزیه شود تا هوای تنفسی تشکیل شود. چگالی بالا و فشار ذخیرهسازی کم آن (زمانی که در دمای پایین نگهداری میشود) آن را قادر میسازد تا با سیستمهای ذخیرهسازی گاز فشار بالا رقابتی بالایی داشته باشد[4]
در سال ۱۹۱۴، رابرت گدارد، پیشگام موشک آمریکایی، اکسید نیتروژن و بنزین را به عنوان پیشرانههای احتمالی برای موشکهای با سوخت مایع پیشنهاد کرد
اکسید نیتروژن اکسید کننده انتخابی در چندین طرح موشک هیبریدی (با استفاده از سوخت جامد با اکسید کننده مایع یا گاز) بودهاست. ترکیب اکسید نیتروژن با سوخت پلی بوتادین با پایانه هیدروکسیل توسط SpaceShipOne و دیگران استفاده شدهاست. همچنین بهطور قابل توجهی در موشکهای آماتور و پرقدرت با پلاستیکهای مختلف به عنوان سوخت استفاده میشود.
اکسید نیتروژن همچنین ممکن است در یک موشک تک پیشران استفاده شود. در حضور یک کاتالیزور گرم شده، N۲O در دمای تقریباً ۱۰۷۰ درجه فارنهایت (۵۷۷ درجه سانتیگراد) بهطور گرمازا به نیتروژن و اکسیژن تجزیه میشود