
Óxido de calcio
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Óxido de calcio?
Resumir este artículo para un niño de 10 años
MOSTRAR TODAS LAS PREGUNTAS
La cal[2] es un término que designa todas las formas físicas en las que puede aparecer el óxido de calcio (CaO). Se obtiene como resultado de la calcinación de las rocas calizas o dolomías.
Datos rápidos Nombre IUPAC, General ...
 | ||
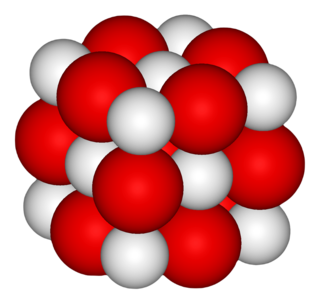 Estructura tridimensional. | ||
| Nombre IUPAC | ||
| Óxido de calcio | ||
| General | ||
| Otros nombres |
Óxido cálcico Óxido de calcio (II) Cal viva | |
| Fórmula molecular | CaO | |
| Identificadores | ||
| Número CAS | 1305-78-8[1] | |
| Número RTECS | EW3100000 | |
| ChEBI | 31344 | |
| ChEMBL | CHEMBL2104397 | |
| ChemSpider | 14095 | |
| DrugBank | 15648 | |
| PubChem | 14778 | |
| UNII | C7X2M0VVNH | |
| KEGG | D01679 C13140, D01679 | |
| Propiedades físicas | ||
| Apariencia | Blanco | |
| Densidad | 3300 kg/m³; 3,3 g/cm³ | |
| Masa molar | 561 g/mol | |
| Punto de fusión | 2845 K (2572 °C) | |
| Punto de ebullición | 3123 K (2850 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 1.19 g/L (25 °C), reacciona | |
| Termoquímica | ||
| ΔfH0gas | 43,93 kJ/mol | |
| ΔfH0líquido | -557,33 kJ/mol | |
| ΔfH0sólido | -635,09 kJ/mol | |
| S0gas, 1 bar | 219,71 J·mol–1·K | |
| S0líquido, 1 bar | 62,31 J·mol–1·K–1 | |
| S0sólido | 39,79 J·mol–1·K–1 | |
| Peligrosidad | ||
| NFPA 704 |
0
3
2
| |
| Frases R | R37, R38, R41 | |
| Frases S | S2, S25, S26, S37, S39 | |
| Frases H | H315, H318, H335 | |
| Frases P | P102, P280, P305+P351+P310, P302+P352, P261, P304+P340, P501 | |
| Riesgos | ||
| Ingestión | Peligroso, causa irritación, en grandes dosis puede ser fatal. | |
| Inhalación | Peligroso; causa irritación, bronquitis química o la muerte en casos de exposición a largo plazo. | |
| Piel | Irritación y posibles quemaduras. | |
| Ojos | Puede causar daños permanentes. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Cerrar
La cal se ha usado desde la más remota Antigüedad como conglomerante en la construcción, también para pintar muros y fachadas de los edificios construidos con adobes o tapial —típico en las antiguas viviendas mediterráneas— o en la fabricación de fuego griego.
