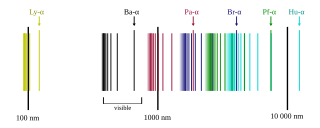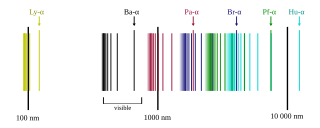Rydbergs formel beskriver emissionsspektret fra brint og brint-lignende ioner . Den udsendte bølgelængde
λ
{\displaystyle \lambda }
1
λ
=
R
H
(
1
n
2
−
1
m
2
)
;
n
<
m
{\displaystyle {\frac {1}{\lambda }}=R_{\mathrm {H} }\left({\frac {1}{n^{2}}}-{\frac {1}{m^{2}}}\right);{\text{ }}n<m}
Hydrogen-spektret på en logaritmisk skala .hvor
R
H
=
10.973.731
,
6
m
−
1
≈
1
,
097
⋅
10
7
m
−
1
{\displaystyle R_{\mathrm {H} }=10.973.731,\!6\,{\text{m}}^{-1}\approx 1,097\cdot 10^{7}\,{\text{m}}^{-1}}
Rydbergs konstant , mens
n
{\displaystyle n}
m
{\displaystyle m}
heltal . For brint-lignende ioner, hvor der stadig kun er én elektron , men kernen har en ladning på
Z
{\displaystyle Z}
elementarladninger , er formlen givet ved:
1
λ
=
Z
2
R
H
(
1
n
2
−
1
m
2
)
;
n
<
m
{\displaystyle {\frac {1}{\lambda }}=Z^{2}R_{\mathrm {H} }\left({\frac {1}{n^{2}}}-{\frac {1}{m^{2}}}\right);{\text{ }}n<m}
Formlen blev formuleret af den svenske fysiker Johannes Rydberg i 1888 .[1]