Fluorid vápenatý
chemická sloučenina / From Wikipedia, the free encyclopedia
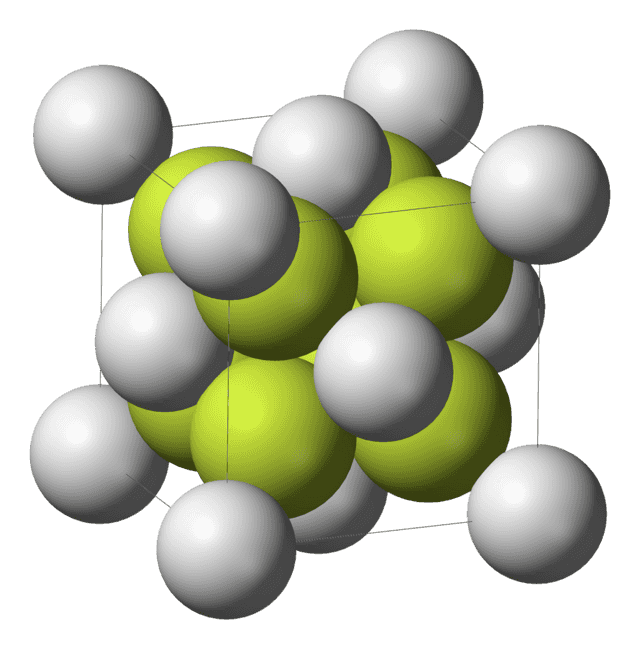
Fluorid vápenatý (CaF2) je iontová sloučenina vápníku a fluoru. Je téměř nerozpustná ve vodě. V přírodě se vyskytuje nejčastěji jako fialový nebo zelenomodrý nerost fluorit (kazivec) a je zdrojem většiny světového fluoru. Tato pevná látka má plošně centrovanou krychlovou strukturu, kde je vápník umístěn mezi osm fluoridových aniontů a každý F− je obklopen čtyřmi ionty Ca2+.[2] Přestože jako čistá látka je bezbarvý, jako minerál je zbarven díky přítomnosti F-center.
Stručná fakta Obecné, Systematický název ...
| Fluorid vápenatý | |
|---|---|
 Krystalická mřížka | |
 Práškový fluorid vápenatý | |
| Obecné | |
| Systematický název | Fluorid vápenatý |
| Anglický název | Calcium fluoride |
| Německý název | Calciumfluorid |
| Sumární vzorec | CaF2 |
| Vzhled | Bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7789-75-5 |
| EC-no (EINECS/ELINCS/NLP) | 232-188-7 |
| Číslo RTECS | EW1760000 |
| Vlastnosti | |
| Molární hmotnost | 78,08 g/mol |
| Teplota tání | 1 360 °C |
| Teplota varu | 2 500 °C |
| Hustota | 3,18 g/cm3 |
| Rozpustnost ve vodě | 0,001 6 g/100 g (18 °C) 0,001 7 g/100 g (26 °C) |
| Součin rozpustnosti | 2,69×10−11 |
| Relativní permitivita εr | 7,36 |
| Měrná magnetická susceptibilita | −4,26 Sm−1 |
| Struktura | |
| Krystalová struktura | Krychlová plošně centrovaná |
| Hrana krystalové mřížky | a=548,6 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −1 214,6 kJ/mol |
| Standardní molární entropie S° | 68,87 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −1 161,9 kJ/mol |
| Izobarické měrné teplo cp | 0,887 JK−1g−1 |
| Bezpečnost | |
| [1] Varování[1] | |
| R-věty | Žádné nejsou |
| S-věty | Žádné nejsou |
| Teplota vznícení | Není vznětlivý |
Některá data mohou pocházet z datové položky. | |
Zavřít
