
Monòxid de carboni
gas incolor, inodor i insípid que és una mica més lleuger que l'aire / From Wikipedia, the free encyclopedia
El monòxid de carboni (CO), també anomenat òxid carbonós, és un gas incolor, inodor i insípid que és una mica més lleuger que l'aire. És altament tòxic pels humans i els animals en grans quantitats, tot i que també és produït en el metabolisme normal dels animals en baixes quantitats, i es creu que té algunes funcions biològiques normals.
| «CO» redirigeix aquí. Vegeu-ne altres significats a «CO (desambiguació)». |
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 27,99491462 Da |
| Trobat en el tàxon | |
| Rol | antimetabòlit, Molècules gasoses de senyalització, tòxic per al desenvolupament i metabòlit primari |
| Estructura química | |
| Fórmula química | CO |
 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Densitat | 0,00125 g/cm³ |
| Velocitat del so | 338 m/s (0 °C, gas) |
| Solubilitat | 2 g/100 g (aigua, 20 °C) |
| Moment dipolar elèctric | 0,11 D |
| Punt de fusió | −205 °C −205 °C |
| Punt d'ebullició | −192 °C (a 760 Torr) −191,5 °C (a 101,325 kPa) |
| Entropia molar estàndard | 197,7 J/(mol K) |
| Moment dipolar elèctric | 0,11 D |
| Entalpia estàndard de formació | −110,52 kJ/mol |
| Pressió de vapor | 35 atm (a 20 °C) |
| Perill | |
| Límit inferior d'explosivitat | 12,5 vol% |
| Límit superior d'explosivitat | 74 vol% |
| Límit d'exposició mitjana ponderada en el temps | 40 mg/m³ (10 h, cap valor) 55 mg/m³ (8 h, Estats Units d'Amèrica) |
| Límit d'exposició sostre | 229 mg/m³ (cap valor) |
| IDLH | 1.380 mg/m³ |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |
| Altres | |
| incolor, inodor, sense sabor i gas inflamable | |
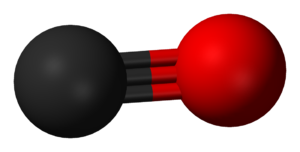
Consisteix d'un àtom de carboni i un àtom d'oxigen, connectats mitjançant un triple enllaç que consisteix en dos enllaços covalents i d'un enllaç covalent datiu. És l'oxocarbonat més simple, i és un anhidre de l'àcid fòrmic.[1] En complexes de coordinació, el lligand del monòxid de carboni s'anomena carbonil.
El monòxid de carboni és produït a partir de l'oxidació parcial dels compostos que contenen carboni; es produeix quan no hi ha suficient oxigen per a produir diòxid de carboni (CO₂), com quan funciona una estufa o en un motor de combustió interna en un espai tancat. En presència d'oxigen, una flama blava crema el monòxid de carboni, donant lloc a diòxid de carboni.[2] El gas d'hulla, que va ser molt utilitzat abans de la dècada dels anys 60 -del segle XX- per a donar llum domèstica, cuinar i escalfar, tot i la seva toxicitat, tenia com a constituent important el CO. Alguns processos en la tecnologia moderna, com per exemple la fusió del ferro, encara produeixen monòxid de carboni com a subproducte.[3]
En tot el món, la font més gran de monòxid de carboni és d'origen natural, a causa de les reaccions fotoquímiques de la troposfera que generen a prop de 5x1012 quilograms a l'any.[4] Altres fonts naturals de CO són els volcans, els incendis forestals, i altres formes de combustió.
En la biologia, el CO es produeix de manera natural per l'acció de les hemo-oxigenases 1 i 2 al grup hemo a partir de la descomposició de l'hemoglobina. Aquest procés produeix una certa quantitat de carboxihemoglobina en persones normals, fins i tot si aquestes no respiren CO. Després de veure per primer cop el 1993,[5] que el CO és un neurotransmissor normal, així com un dels tres gasos (els altres dos són l'òxid nítric i el sulfur d'hidrogen), que modula naturalment respostes inflamatòries en el cos, el CO ha rebut molta atenció clínica com a regulador biològic. Es coneix que els tres gasos actuen com a antiinflamatoris, vasodilatadors i estimuladors del creixement neovascular, en molts teixits.[6] S'estan fent assajos clínics del CO com a medicament en petites quantitats.