
Вада
празрыстая, амаль бясколерная вадкасць без паху і смаку / From Wikipedia, the free encyclopedia
Вада́, або дыяксід вадароду (H2O) — найпрасцейшае ўстойлівае злучэнне вадароду з кіслародам.
Хуткія факты Агульныя, Фізічныя ўласцівасці ...
| Вада | |
 | |
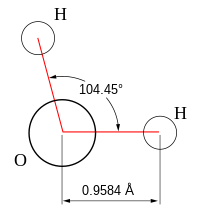 | |
 | |
| Агульныя | |
|---|---|
| Сістэматычнае найменне | Аксід вадароду Вода[1] |
| Традыцыйныя назвы | вада |
| Хім. формула | Н2O |
| Фізічныя ўласцівасці | |
| Стан (ст. ум.) | вадкасць |
| Малярная маса | 18,01528 г/моль |
| Шчыльнасць | 0,9982 г/см³ |
| Дынамічная вязкасць (ст. ум.) | 0,00101 Па·с (пры 20 °C) |
| Кінематычная вязкасць (ст. ум.) | 0,01012 см²/с (при 20 °C) |
| Тэрмічныя ўласцівасці | |
| Тэмпература плаўлення | 0 °C |
| Тэмпература кіпення | 99,974 °C |
| Патройны пункт | 0,01 °C, 611,73 Па |
| Крытычны пункт | 374 °C, 22,064 МПа |
| Малярная цеплаёмістасць (ст. ум.) | 75,37 Дж/(моль·К) |
| Цеплаправоднасць (ст. ум.) | 0,56 Вт/(м·K) |
| Класіфікацыя | |
| Рэг. нумар CAS | 7732-18-5 |
| PubChem | 962; 22247451 |
| Рэг. нумар EINECS | 231-791-2 |
| SMILES | |
| RTECS | ZC0110000 |
| ChemSpider | 937 |
Закрыць

Старажытныя філосафы лічылі ваду адным з чатырох першасных элементаў. Такія ўяўленні існавалі і ў Сярэднявеччы. Утварэнне вады пры згаранні вадароду было даведзена Г. Кавендышам (1781). Хімічная формула была канчаткова ўстаноўленая С. Каніцара (1860).