
സോഡിയം ഹൈഡ്രോക്സൈഡ്
രാസസംയുക്തം / From Wikipedia, the free encyclopedia
ഫലകം:Chembox E number
വസ്തുതകൾ Names, Identifiers ...
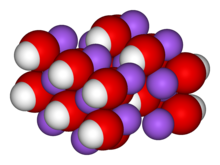 | |
 | |
| Names | |
|---|---|
| Preferred IUPAC name
Sodium hydroxide[1] | |
| Systematic IUPAC name
Sodium oxidanide[2] | |
| Other names | |
| Identifiers | |
3D model (JSmol) |
|
| ChEBI | |
| ChemSpider |
|
| ECHA InfoCard | 100.013.805 |
| EC Number |
|
| Gmelin Reference | 68430 |
| KEGG |
|
| MeSH | {{{value}}} |
PubChem CID |
|
| RTECS number |
|
| UNII | |
| UN number | 1824 |
CompTox Dashboard (EPA) |
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | White, waxy, opaque crystals |
| Odor | odorless |
| സാന്ദ്രത | 2.13 g/cm3 |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| 418 g/L (0 °C) 1110 g/L (20 °C) 3370 g/L (100 °C) | |
| Solubility | soluble in glycerol negligible in ammonia insoluble in ether slowly soluble in propylene glycol |
| Solubility in methanol | 238 g/L |
| Solubility in ethanol | <<139 g/L |
| ബാഷ്പമർദ്ദം | <2.4 kPa (at 20 °C) |
| Basicity (pKb) | -0.56 (NaOH(aq) = Na+ + OH–) [5] |
| −16.0·10−6 cm3/mol | |
| Refractive index (nD) | 1.3576 |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−427 kJ·mol−1[6] |
| Standard molar entropy S |
64 J·mol−1·K−1[6] |
| Specific heat capacity, C | 59.66 J/mol K |
| Hazards | |
| Safety data sheet | External MSDS |
| GHS pictograms |  |
| GHS Signal word | Danger |
GHS hazard statements |
H290, H314 |
GHS precautionary statements |
P280, P305+351+338, P310 |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose) |
40 mg/kg (mouse, intraperitoneal)[7] |
LDLo (lowest published) |
500 mg/kg (rabbit, oral)[8] |
| NIOSH (US health exposure limits): | |
PEL (Permissible) |
TWA 2 mg/m3[9] |
REL (Recommended) |
C 2 mg/m3[9] |
IDLH (Immediate danger) |
10 mg/m3[9] |
| Related compounds | |
| Other anions | Sodium hydrosulfide |
| Other cations | Caesium hydroxide Lithium hydroxide |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
അടയ്ക്കുക
ഒരു കോസ്റ്റിക് ലോഹീയ ക്ഷാരമാണ് സോഡിയം ഹൈഡ്രോക്സൈഡ്. വെള്ളം പോലുള്ള ലായകത്തിൽ ലയിപ്പിക്കുമ്പോൾ ശക്തിയേറിയ ആൽക്കലൈൻ ലായനി രൂപം കൊള്ളുന്നു.