
Фосфат
сол или естер на фосфорната киселина / From Wikipedia, the free encyclopedia
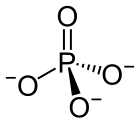
Фосфат — анјон, сол, функционална група или естер на фосфорната киселина. Под ова најчесто се подразбира ортофосфат, изведен од ортофосфорната киселина H3PO4.
 | |||
| |||
| Систематско име | фосфат[1] | ||
| Назнаки | |||
|---|---|---|---|
| 14265-44-2 | |||
| Бајлштајн | 3903772 | ||
| ChEBI | CHEBI:18367 | ||
| ChemSpider | 1032 | ||
Гмелин |
1997 | ||
| 3Д-модел (Jmol) | Слика Слика Слика Слика | ||
| MeSH | Phosphates | ||
| PubChem | 1061 | ||
| |||
| UNII | NK08V8K8HR | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Конјуг. киселина | моноводород фосфат | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Фосфатниот или ортофосфатниот јон [PO4]3− е изведен од фосфорна киселина со отстранување на три протони H+. Со отстранување на еден или два протона се добива диводород фосфат [H2PO4]− и водород фосфат [HPO4]2−. Истите имиња важат и за солите на тие анјони, како што се амониум диводород фосфат и тринатриум фосфат.
- H3PO4
Фосфорна
киселина - [H2PO4]−
Диводород
фосфат - [HPO4]2−
Водород
фосфат - [PO4]3−
Фосфат
Во органската хемија, „фосфат“ или „ортофосфат“ е органофосфат, естер на ортофосфорната киселина од обликот PO4RR′R″ каде еден или повеќе водородни атоми се заменети со органски групи. Таков пример е триметил фосфатот, (CH3)3PO4. Поимот се однесува и на тривалентната функционална група OP(O-)3 кај таквите естри.
Профосфатите имаат особено значење меѓу различните фосфати поради нивните важни улоги во биохемијата, биогеохемијата и екологијата, како и нивната стопанска важност во земјоделството и индустријата.[2] Додавањето и отстранувањето на фосфатни групи (фосфорилација и дефосфорилација) се клучни чекори во клеточниот метаболизам.
Ортофосфатите можат да се кондензираат, образувајќи пирофосфати.



![[H2PO4]−Диводородфосфат](http://upload.wikimedia.org/wikipedia/commons/thumb/d/db/2-dihydrogenphosphate-3D-balls.png/152px-2-dihydrogenphosphate-3D-balls.png)
![[HPO4]2−Водородфосфат](http://upload.wikimedia.org/wikipedia/commons/thumb/8/87/1-hydrogenphosphate-3D-balls.png/123px-1-hydrogenphosphate-3D-balls.png)
![[PO4]3−Фосфат](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b0/0-phosphate-3D-balls.png/120px-0-phosphate-3D-balls.png)