
قانون بویل
قانون علم شیمی / From Wikipedia, the free encyclopedia
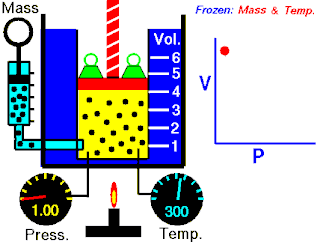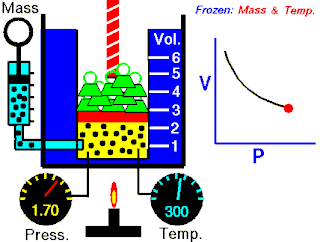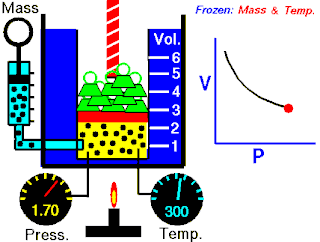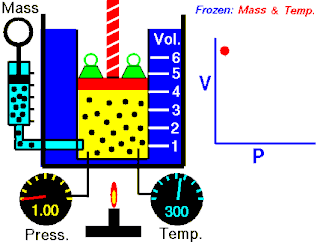
قانون بویل قانونی در علم فیزیک است که بیان میکند در دمای ثابت حجم گازها با وارد شدن فشار بهطور منظمی کاهش مییابد؛ به عبارت دیگر، در گازها همواره میان حجم و فشار رابطهای وارونه وجود دارد. این قانون را دانشمند انگلیسی، رابرت بویل (۱۶۲۷–۱۶۹۱)، کشف کردهاست. این قانون با عنوان قانون بویل–ماریوت نیز شناخته میشود.
که در آن
- p نشان دهنده فشار
- v نشان دهنده حجم
- و k نشان دهنده مقدار ثابت است:
که در آن
- n نشان دهنده تعداد مول
- R نشان دهنده ثابت عمومی گازها
- و T نشان دهنده دمای محیط است.[1]
قانون بویل به این صورت نیز بیان شدهاست:
- که در آن
فشار گاز ایدئال در قبل از فرایند
حجم گاز ایدئال در قبل از فرایند
دمای گاز ایدئال در قبل از فرایند
فشار گاز ایدئال در بعد از فرایند
حجم گاز ایدئال در بعد از فرایند
دمای گاز ایدئال در بعد از فرایند








