
Presión de vapor
De Wikipedia, la enciclopedia encyclopedia
La presión de vapor es la presión que ejerce la fase gaseosa o vapor sobre la fase líquida en un sistema cerrado a una temperatura determinada, cuando la fase líquida y el vapor se encuentran en equilibrio dinámico. Su valor es independiente de las cantidades de líquido y vapor presentes mientras existan ambas. Este fenómeno también lo presentan los sólidos; cuando un sólido pasa al estado gaseoso sin pasar por el estado líquido (proceso denominado sublimación o el proceso opuesto, llamado sublimación inversa o deposición) también hablamos de presión de vapor. En la situación de equilibrio, las fases reciben la denominación de líquido saturado y vapor saturado. Esta propiedad posee una relación directamente proporcional con las fuerzas moleculares, debido a que cuanto mayor sea el módulo de las mismas, mayor deberá ser la cantidad de energía entregada (ya sea en forma de calor u otra manifestación) para vencerlas y producir el cambio de estado.
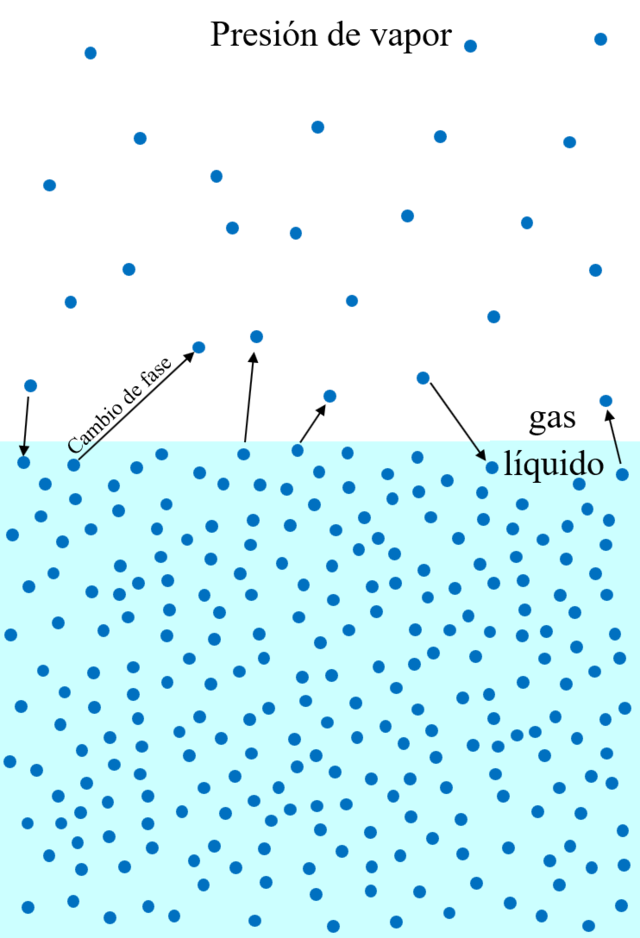

Inicialmente solo se produce la evaporación, ya que no hay vapor; sin embargo, a medida que la cantidad de vapor aumenta, y por tanto la presión en el interior de la ampolla, se va incrementando también la velocidad de condensación, hasta que transcurrido un cierto tiempo ambas velocidades se igualan. Llegado este punto se habrá alcanzado la presión máxima posible en la ampolla (presión de vapor o de saturación): la presión total del volumen de gas (mezcla vapor-aire) es equivalente a la presión parcial de la fase vapor (presión de saturación). Esta presión de saturación solo podrá superarse aportando más energía (temperatura) a la mezcla, acción que incrementaría la presión de vapor (la tasa de evaporación), y a su vez, la presión total de la mezcla (ya que es un recipiente cerrado).
El equilibrio dinámico se alcanzará más rápidamente cuanto mayor sea la superficie de contacto entre el líquido y el vapor, pues así se favorece la evaporación del líquido; del mismo modo que un charco de agua extenso pero de poca profundidad se seca más rápido que uno más pequeño pero de mayor profundidad que contenga igual cantidad de agua. Sin embargo, el equilibrio se alcanza en ambos casos para igual presión.
El factor más importante que determina el valor de la presión de saturación es la propia naturaleza del líquido, encontrándose que, en general, entre líquidos de naturaleza similar, la presión de vapor a una temperatura dada es tanto menor cuanto mayor es la masa molecular del líquido.
Por ejemplo, el aire al nivel del mar saturado con vapor de agua a 20 °C tiene una presión parcial de 23 mbar de agua y alrededor de 780 mbar de nitrógeno, 210 mbar de oxígeno y 9 mbar de argón.
La presión de vapor de cualquier sustancia aumenta de forma no lineal con la temperatura, a menudo descrita por la ecuación de Clausius-Clapeyron. La presión atmosférica [de un líquido (también conocido como punto de ebullición normal) es la temperatura a la que la presión de vapor es igual a la presión atmosférica ambiente. Al aumentar la temperatura, la presión de vapor es suficiente para superar la presión atmosférica y hacer que el líquido forme burbujas de vapor. La formación de burbujas en profundidades de líquido elevadas requiere una temperatura ligeramente superior debido a la mayor presión del líquido, debida a la presión hidrostática de la masa de líquido superior. Más importante a poca profundidad es la mayor temperatura necesaria para iniciar la formación de burbujas. La tensión superficial de la pared de la burbuja provoca una sobrepresión en las burbujas iniciales muy pequeñas.
La presión de vapor que un solo componente de una mezcla aporta a la presión total del sistema se denomina presión parcial. Por ejemplo, el aire a nivel del mar, y saturado de vapor de agua a 20 °C, tiene presiones parciales de unos 2,3 kPa de agua, 78 kPa de nitrógeno, 21 kPa de oxígeno y 0,9 kPa de argón, totalizando 102,2 kPa, lo que constituye la base de la presión atmosférica estándar.