
Óxido de etileno
compuesto químico / De Wikipedia, la enciclopedia encyclopedia
Estimado Wikiwand AI, Seamos breves simplemente respondiendo estas preguntas clave:
¿Puede enumerar los principales datos y estadísticas sobre Óxido de etileno?
Resumir este artículo para un niño de 10 años
El óxido de etileno es un gas inflamable de aroma fuerte de fórmula C
2H
4O. Se disuelve fácilmente en agua.
Es comúnmente usado como esterilizante.
  | ||
 | ||
| Nombre IUPAC | ||
|
Oxirano Oxaciclopropano | ||
| General | ||
| Otros nombres |
Epoxietano Óxido de etileno | |
| Fórmula estructural |
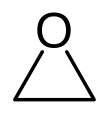 | |
| Fórmula molecular | C2H4O | |
| Identificadores | ||
| Número CAS | 75-21-8[1] | |
| Número RTECS | KX2450000 | |
| ChEBI | 27561 | |
| ChEMBL | CHEMBL1743219 | |
| ChemSpider | 6114 | |
| PubChem | 6354 | |
| UNII | JJH7GNN18P | |
| KEGG | D03474 | |
| Propiedades físicas | ||
| Densidad | 899 kg/m³; 0,899 g/cm³ | |
| Masa molar | 44,05 g/mol | |
| Punto de fusión | 161PFC=-112.1 | |
| Punto de ebullición | 283,5 K (10 °C) | |
| Índice de refracción (nD) | 1,35965 | |
| Propiedades químicas | ||
| Solubilidad en agua | Miscible | |
| Peligrosidad | ||
| NFPA 704 |
4
3
3
| |
| Límites de explosividad | 3.6 - 100%[3] | |
| Riesgos | ||
| Inhalación | Irritación pulmonar, convulsiones. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
También denominado Oxirano; 1,2-epoxietano; Óxido de dimetilo; dihidroxioxirano; OE.
El óxido de etileno es un gas incoloro e inflamable a temperaturas y presiones normales, pero se condensa cuando es enfriado. Los vapores de óxido de etileno forman mezclas explosivas con el aire. Es miscible con el agua en cualquier proporción, con alcohol, éter y la mayoría de disolventes orgánicos. Es muy reactivo tanto en fase líquida como vapor.
A 0 °C es un líquido transparente, incoloro y libre de sedimento o turbidez.
Se trata de una sustancia química usada principalmente para fabricar glicol de etileno (una sustancia química usada como anticongelante y poliéster). El óxido de etileno se ha fabricado usando dos procesos diferentes: uno, ya en desuso, por vía clorhidrina y otro vía oxidación directa (usado en la actualidad por las plantas que lo producen). En este proceso se oxida catalíticamente con plata el etileno con oxígeno para la formación del óxido de etileno. El oxígeno puede proceder del aire atmosférico (21%) o bien utilizando oxígeno de alta pureza (mayor de un 95 %). Desde el año 2000 las nuevas plantas que se construyen utilizan oxígeno puro en la reacción de oxidación para obtener un mayor rendimiento.
Las dos reacciones principales que se producen son:
C2H4+ 0,5O2→C2H4O Combustión parcial, ligeramente exotérmica
C2H4+ 3O2→2CO2+ 2H2O Combustión total, fuertemente exotérmica.
Su principal consumo es la fabricación de etilenglicoles (alrededor del 60% del óxido de etileno mundial es convertido a monoetilenglicol y un 13% se destina a di, tri y polientilenglicol). Una pequeña cantidad (menos de 1%) es usada para controlar insectos en ciertos productos agrícolas almacenados, y una cantidad muy pequeña se usa en hospitales para esterilizar equipo y abastecimientos médicos.[4][5]
