أكسيد النيتروس
مركب كيميائي / من ويكيبيديا، الموسوعة encyclopedia
عزيزي Wikiwand AI, دعنا نجعلها قصيرة من خلال الإجابة ببساطة على هذه الأسئلة الرئيسية:
هل يمكنك سرد أهم الحقائق والإحصائيات حول أكسيد النيتروز?
تلخيص هذه المقالة لعمر 10 سنوات
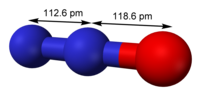
أكسيد النيتروس يعرف أيضا بأكسيد النيتروجين الثنائي أو أحادي أكسيد ثنائي النيتروجين وهو مشهور باسم غاز الضحك لأثاره المنشطة عند استنشاقه، وهو مركب كيميائي بالصيغة الكيميائية N2O، في الحالة الطبيعية هو غاز عديم اللون، غير قابل للاشتعال، له رائحة محببة للنفس، شبه حلوة. يستخدم في الجراحة وطب الأسنان لأثاره المسكنة والمخدرة. ويستعمل أكسيد النيتروس كوسيلة لتفعيل فترات قصيرة من الأداء الفائق في محركات الحرق الداخلي في السيارات، وذلك يتم بإدخال أكسجين إضافي إلى الشحنة الداخلة والذي بالتالي يسمح بدخول كمية أكبر من الوقود الذي يتم حرقه وزيادة الكمية الناتجة من الطاقة بشكل مطرد، مؤدياً إلى زيادة القوة التي ينتجها المحرك. أكسيد النيتروس موجود في الهواء ويعد من غازات الدفيئة.
| أكسيد النيتروس | |
|---|---|
| أسماء أخرى | |
Nitrous oxide | |
| المعرفات | |
| رقم CAS | 10024-97-2 |
| بوب كيم (PubChem) | 948 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | N2O |
| الكتلة المولية | 44.0128 g/mol |
| المظهر | colorless gas |
| الكثافة | 1222.8 kg m-3 (liquid) 1.8 kg m-3 (gas STP) |
| نقطة الانصهار | -90.86 °س، 182 °ك، -132 °ف |
| نقطة الغليان | -88.48 °س، 185 °ك، -127 °ف |
| البنية | |
| البنية الجزيئية | linear |
| عزم جزيئي ثنائي القطب | 0.166ديباي |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
+82.05 |
| إنتروبيا مولية قياسية S |
219.9 جول لكل مول كلفن[3] |
| علم الأدوية | |
| طريق التناول | شهيق |
| الاستقلاب | 0.004% |
| Elimination half-life |
5 minutes |
| إخراج | جهاز تنفسي |
| الوضع القانوني | {{{legal_status}}} |
| المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
|
| مركبات متعلقة | |
| مركبات ذات علاقة | أحادي أكسيد النيتروجين، ثنائي أكسيد النيتروجين، ثلاثي أكسيد ثنائي النتروجين، رباعي أكسيد ثنائي النتروجين، خماسي أكسيد ثنائي النتروجين، حمض النتريك، حمض النتروز |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |